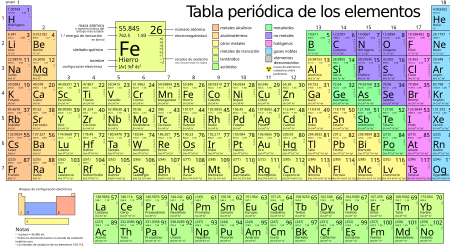
Importancia de los electrones de valencia en química
Los electrones de valencia son fundamentales en el estudio de la química, ya que son los responsables de las interacciones que tienen los átomos entre sí para formar compuestos. Estos electrones determinan las propiedades químicas de un elemento y su capacidad para unirse con otros átomos. Es por ello que comprender el concepto de electrones de valencia es esencial para entender la estructura y comportamiento de los elementos en la tabla periódica.
¿Qué son los electrones de valencia?
Los electrones de valencia son los electrones más externos de un átomo, es decir, aquellos que se encuentran en la capa de mayor energía. Estos electrones son los responsables de las reacciones químicas y de la formación de enlaces entre átomos. La cantidad de electrones de valencia de un elemento determina su valencia, es decir, su capacidad para combinarse con otros elementos.
Importancia en la formación de compuestos
Los electrones de valencia son clave en la formación de compuestos químicos, ya que son estos electrones los que participan en la creación de enlaces químicos. Cuando dos átomos se unen para formar un compuesto, los electrones de valencia de cada átomo interactúan entre sí para establecer los enlaces químicos necesarios. Dependiendo de la cantidad de electrones de valencia que posea un átomo, este podrá compartir, perder o ganar electrones para completar su capa de valencia y adquirir estabilidad.
¿Por qué se le llama capa de valencia?
La capa de valencia recibe su nombre debido a que es en esta capa donde se encuentran los electrones de valencia de un átomo. Esta capa es la más externa y la de mayor energía en la estructura de un átomo, y es donde residen los electrones que determinan la reactividad química del elemento. La capa de valencia es crucial en la formación de compuestos, ya que al interactuar los electrones de valencia de diferentes átomos se establecen los enlaces químicos que dan lugar a las moléculas.
Interacción de los electrones de valencia
Los electrones de valencia de un átomo pueden interactuar de diferentes maneras con los electrones de valencia de otros átomos. Esta interacción puede darse a través de enlaces iónicos, enlaces covalentes o enlaces metálicos, dependiendo de la naturaleza de los átomos involucrados y de su tendencia a ganar, perder o compartir electrones. La capacidad de los electrones de valencia para establecer enlaces es lo que permite la formación de una amplia variedad de compuestos químicos con propiedades únicas.
Descubre el origen de los electrones de valencia
Los electrones de valencia tienen su origen en la configuración electrónica de un átomo, la cual determina la distribución de los electrones en las distintas capas o niveles de energía. Cada nivel de energía puede contener un máximo de electrones, y los electrones de valencia son aquellos que se encuentran en el nivel más externo. La distribución de estos electrones en la capa de valencia es lo que define las propiedades químicas de un elemento y su capacidad para formar enlaces con otros elementos.
Configuración electrónica y electrones de valencia
La configuración electrónica de un átomo se representa mediante una notación que indica la distribución de electrones en los distintos niveles de energía. Los electrones de valencia se identifican fácilmente observando el último número en la configuración electrónica de un elemento. Por ejemplo, en el caso del carbono cuya configuración electrónica es 1s2 2s2 2p2, los electrones de valencia son los dos electrones en el nivel 2p, ya que son los más externos y determinan la reactividad del átomo.
¿Qué se entiende por valencia? Descúbrelo aquí
En química, la valencia es la capacidad de un átomo para combinarse con otros átomos mediante la formación de enlaces químicos. La valencia de un elemento está determinada por la cantidad de electrones de valencia que posee, es decir, por la cantidad de electrones en la capa más externa de su estructura electrónica. Esta propiedad es fundamental para predecir cómo un átomo reaccionará con otros átomos y qué tipo de enlace formará.
Relación entre valencia y electrones de valencia
La valencia de un elemento químico está estrechamente relacionada con la cantidad de electrones de valencia que tiene. Los elementos con la misma cantidad de electrones de valencia tienden a tener propiedades químicas similares y a formar compuestos de manera parecida. Por ejemplo, todos los elementos del grupo 17 de la tabla periódica tienen 7 electrones de valencia y tienden a ganar un electrón para completar su capa de valencia, formando así enlaces iónicos con otros elementos.
Aplicaciones de la valencia en química
La valencia de un elemento es una propiedad fundamental en química que se utiliza para predecir su comportamiento químico y su capacidad para formar compuestos. Conocer la valencia de un elemento permite determinar cómo se combinan los átomos para formar moléculas, qué tipo de enlaces se establecen y cuál será la estructura final del compuesto resultante. Esta información es esencial en la síntesis de nuevos materiales, en la industria farmacéutica y en la investigación química en general.
Preguntas frecuentes
1. ¿Por qué los electrones de valencia son tan importantes en química?
Los electrones de valencia son fundamentales en química porque son los responsables de las interacciones entre átomos que dan lugar a la formación de compuestos y moléculas. Son estos electrones los que determinan las propiedades químicas de un elemento y su capacidad para unirse con otros elementos.
2. ¿Cómo se relacionan la valencia y los electrones de valencia?
La valencia de un elemento está determinada por la cantidad de electrones de valencia que posee. Cuantos más electrones de valencia tenga un átomo, mayor será su valencia y mayor será su capacidad para combinarse con otros átomos mediante la formación de enlaces químicos.
3. ¿Qué sucede si un átomo pierde o gana electrones de valencia?
Cuando un átomo pierde o gana electrones de valencia, su carga eléctrica se modifica y se convierte en un ion positivo (si pierde electrones) o negativo (si gana electrones). Estos iones pueden interaccionar con otros iones de carga opuesta para formar compuestos iónicos estables.
4. ¿Cómo influye la valencia en la reactividad química de un elemento?
La valencia de un elemento determina su capacidad para reaccionar con otros elementos y formar compuestos. Elementos con valencias similares tienden a comportarse de manera parecida químicamente, ya que buscan adquirir la configuración electrónica más estable a través de la formación de enlaces.
5. ¿Por qué es importante conocer la valencia de los elementos en la química aplicada?
Conocer la valencia de los elementos es fundamental para comprender cómo se combinan y reaccionan en distintas situaciones químicas. Esta información es esencial en la síntesis de compuestos, en la formulación de medicamentos y en el diseño de nuevos materiales con propiedades específicas.